アポトーシス、反発性アポトーシスと脳の発達障害
【シリーズ重点研究プログラムの紹介:
「化学物質評価・管理イノベーション研究プログラム」から】
石堂 正美
アポトーシスという言葉はギリシャ語に由来しapo(離れて)とptosis(落ちる)の合成語で木の葉や花弁がおちるという意味をもち、一つの細胞死を表す言葉として1972年スコットランドの病理学者によって提唱されました。彼らがアポトーシスという細胞死を提唱する前まではネクローシス(壊死)という細胞死についての研究がなされてきました。正常な組織や器官が退縮するときや、発生過程の組織、病理的な組織変化などを顕微鏡による観察を通じてネクローシスとは異なる細胞死像に彼らは気付いたのです。彼らが提唱したアポトーシスという細胞死が俄然注目されることになったのは、アポトーシスに関連する哺乳類遺伝子が1993年に見つかったことに因ります。細胞の死の運命はもともとプログラムされているというのですから、強烈なインパクトを与えました。
一方で、重金属や化学物質による細胞レベルでの細胞死は従来ネクローシスとして研究されてきました。1950~60年代に深刻化したイタイイタイ病の原因物質であるカドミウムも水俣病の原因物質であるメチル水銀も標的臓器の細胞をネクローシスにより損傷を与えるものとして研究報告されてきました。顕微鏡で見たネクローシスの形態変化は、細胞質の細胞小器官が膨らみ、細胞全体も膨らみやがて細胞の内容物が漏出するように観察されます。こうした背景の中、カドミウムの毒性を研究することになった筆者は、カドミウムによるアポトーシスの誘導を見出しました。ちょうど、1993年のことで、発生学分野では個体発生におけるプログラムされたアポトーシス研究が急速な進展を見せた頃です。この新たな知見が国内外の毒性学分野を席巻したことを思いだします。1つの重金属がアポトーシスとネクローシスを誘導しますが、重金属の毒性が弱いときや毒性発現の初期段階でアポトーシスが観察されると考えられており、DNAの断片化やクロマチンの凝縮が観察されます。したがって、今日では重金属に限らず化学物質の毒性の早期検出の指標としてのアポトーシスが活用されています。
さて、反発性アポトーシスは、筆者の造語で、英語はrepulsive apoptosisとして論文は受理されました。具体的には、神経系細胞が移動しているときナノ材料である銀ナノ粒子との接触によりアポトーシスが誘導され結果的に神経系細胞の移動が後退し、この時のアポトーシスを反発性アポトーシスと呼びました。この知見は、本重点プロジェクトにおいてナノ材料の神経系毒性評価を行った際に見出したものです。ナノは長さを表し(10-9m)、この領域で行われている科学技術がナノテクノロジーですが、物理学的にも特異的な位置づけがなされています。これまでの物理学の成果は自然の普遍的構造の統一的理解ではなく、自然をサブ構造的に理解することでした。内容的には、古典力学、量子力学、熱力学そして統計力学といったものによりそれぞれの側面の普遍的構造が記述されてきました。ナノ領域はちょうど古典力学と量子力学の境界に位置し、量子力学的物性が表れはじめるとされ、新たな研究領域として注目され続けてきています。
ナノ材料では結晶のサイズが小さくなることにより、電子状態が変化し、通常の大きな物質にはないような性質が現れます。化学反応は、基本的に物質の表面で起こりますが、物質がナノサイズになることにより単位質量当たりの表面積が大きくなります。この比表面積の増大が化学的反応性を高めます。その他、小さくなることにより多くの物理化学的な変化が知られてきていますが、身体の中での生物学的な作用は必ずしも明らかになっていません。そこで、本プロジェクトでは神経系細胞の根幹と考えられている神経幹細胞を用いたニューロスフェア法で銀ナノ粒子の神経系発生毒性評価を行いました。
神経幹細胞は自己増殖能をもち、様々な神経系細胞に分化できる多分化能を有し中枢神経系の発生に重要な役割を演じています。脳・神経系が構築されるには、発生過程において神経系細胞が移動し精緻な組織構造を形成し、維持されることが必要です。胎児期から生後にわたるこうした組織構造、回路形成と維持に異常をきたすと、脳の発達障害を生じます。
はじめにラット胎生15~16日の中脳胞から神経幹細胞を単離し、その培養系を確立しました。中脳胞から取り出した神経幹細胞は、自己組織化により培養7日ぐらいから塊を形成しはじめ、2~3週間で直径100~200ミクロンの球状の塊を形成します(これをニューロスフェアと呼びます)。今回は、このニューロスフェアを用いて実験を行いました。ニューロスフェアを培養系に静置すると、表面から細胞が飛び出してきます。ニューロスフェアが培養皿に接着していると、飛び出してくる細胞も底皿を外側に向かって移動していくことが観察されました。脳内の細胞移動と培養系の細胞移動が同義的とは考えにくいですが、現象的に模倣します。
次に、こうした系に銀ナノ粒子を曝露し、その影響を調べました。ある濃度以上の銀ナノ粒子を曝露すると、ニューロスフェアから移動してくる細胞が少なくなることに気づきました。細胞の移動距離を測定し、銀ナノ粒子濃度との関係を調べてみますと、直線関係を得ることができました。50%阻害率(IC50)を見積もると、約400 ng/mlでした。これは他の細胞を用いた研究報告よりも大変感度の良い評価系であることを示しています。
また、銀ナノ粒子を曝露する前に予めニューロスフェアから神経幹細胞を十分に移動させておき、それから銀ナノ粒子を曝露する実験を行いました。そうしますと、ある濃度以上の銀ナノ粒子は、移動した神経幹細胞のアポトーシスを誘導させることが明らかになりました(図)。結果的に移動した神経幹細胞が反発し縮退したかのようになります(反発性アポトーシス)。細胞骨格を調べてみますと細胞の形態が変化し、細胞内小器官の一つであるミトコンドリアの膜電位の異常も付随して観察されました。
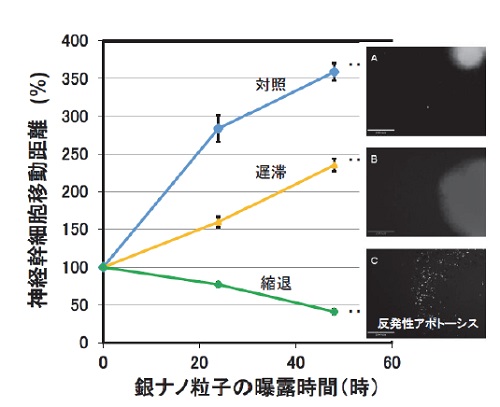
右写真:アポトーシスが誘導されると断片化したDNAが標識される方法を用いて、それぞれの場合でのアポトーシス誘導の有無を調べてみると、縮退の時のみにアポトーシス誘導が観察された(写真C)。スケール・バー 200 μm。
一般的に、アポトーシスは不要になった細胞の除去機構として考えられてきました。近年ではアポトーシス現象に代償性増殖という現象が付随することがわかり、アポトーシスは損傷修復による恒常性の維持機構に関与していることが示唆され、その概念が拡張してきています。反発性アポトーシスの意義については現在のところ不明です。脳の形成にとって最も重要なことは組織構造と神経回路が精緻に形成されることです。そのために脳の中には誘導性因子や反発性因子が存在し正しいガイドがなされています。この類似性から、銀ナノ粒子には細胞移動に対して反発させる性質があることが示されたわけです。このことは、脳の発達過程で銀ナノ粒子が脳内に取り込まれたときに精緻な組織構造や神経系回路網が障害されることを容易に想像させます。
神経細胞移動障害として滑脳症や脳の発達障害が注目されてきており、実際、銀ナノ粒子を新生期の仔ラットの口に含ませると、脳の発達障害がみられることも私たちの研究からもわかってきました。この点の詳細はまたの機会に紹介したいと思います。
執筆者プロフィール

学術的な情報が惜しみなく提供されているインターネットは新しい学びの場で、現代版リベラル・アーツになっています。閲覧フリーが多い中、書籍代の経費節約にはならず逆に出費がかさんでいますが、広く自然科学を学ぶためのpower on。


