コプラナーPCBと薬物代謝酵素
研究ノート
松本 理
ポリ塩化ビフェニル(PCB)は日本では1968年に発生した油症事件の原因物質として知られている。その毒性と蓄積性のために1972年以降生産と使用が中止されているが,現在も環境中に残留していることが問題となっている。PCBの中で,塩素原子がベンゼン環に結合している位置により扁平構造をとることが可能な異性体はコプラナーPCBと呼ばれ,毒性が強い。コプラナーPCBはまたマウスやラットの肝臓などで発癌性を示すが,その発癌性は癌化を促進する作用(プロモーション)によると考えられている。コプラナーPCBはポリ塩化ジベンゾ-p-ジオキシン(PCDD)やポリ塩化ジベンゾフラン(PCDF)と類似の構造を持っており,ダイオキシン類の中に加えられている。環境中に存在するダイオキシン類の中で,コプラナーPCBが多くの割合を占めているとされている。
さて,ダイオキシン類のような異物が生体内に入ってきたときに,生体内では薬物代謝酵素とよばれるいくつかの酵素が誘導される。これは生体内に入ってきた異物を無害なものに変え,体外に排泄しようとする生体の反応であると考えられる。しかし,薬物代謝酵素は異物を無害化するばかりではなく,ときには取り込まれた物質を発癌性などの毒性のある活性代謝物に変えてしまうこともあるからその作用は複雑である。
薬物代謝酵素には大きく分けて2段階の酵素が存在する。第1段階の薬物代謝酵素は主に酸化酵素で,第1相酵素とよばれる。第1相酵素の代表は肝臓のミクロソームなどに存在するチトクロームP450とよばれる酵素群である。チトクロームP450はコプラナーPCBを初めとする多くの化学物質によって誘導されるが,その誘導の機構は細胞内に存在するAh(アリルハイドロカーボン)受容体を介するものであることはよく知られている。遺伝子(DNA:デオキシリボ核酸)上の情報はmRNA(メッセンジャー・リボ核酸)に転写され,さらにその情報をもとにしてタンパク質が合成されるのであるが,遺伝子上にはmRNAへの転写を調節するための領域も存在する。コプラナーPCBなどの異物はAh受容体と結合したのち,チトクロームP450の遺伝子の調節領域にある異物応答配列(xenobiotic responsive element:XRE)とよばれる部分に作用してチトクロームP450の転写を起こす(図)。
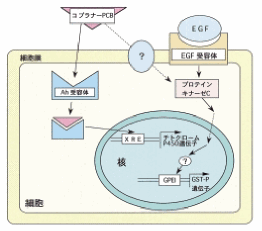
GST-P:P型グルタチオンS-トランスフェラーゼ,
GPEI:GST-PエンハンサーI,XRE:異物応答配列
第2段階の薬物代謝酵素には還元酵素や抱合酵素などがある。抱合酵素のひとつ,P型グルタチオンS-トランスフェラーゼ(GST-P)は正常なラットの肝臓の細胞には存在しないが,ラットの肝癌細胞では発現し,ラットの肝癌のマーカー酵素として知られている。
筆者らはコプラナーPCBの作用によりGST-Pが誘導されること,さらにコプラナーPCBによるGST-Pの誘導には,GST-P遺伝子の調節領域にあるGST-PエンハンサーI(GPE I)とよばれる配列が必要であることを,ラットの正常な肝臓の培養細胞を用いて明らかにしてきた(図)。
一方,ブチルヒドロキシアニソールのような酸化ストレスを防御する働きをもつ抗酸化剤によって誘導される別の第2相酵素であるNAD(P)H:キノンオキシドリダクターゼの遺伝子の調節領域には,抗酸化剤応答配列(antioxidant responsive element:ARE)とよばれる配列が含まれている。AREは抗酸化剤によるこの酵素の発現に必要な領域であることがわかっている。
ところが,このAREの配列がGPE Iの配列とよく似ていることがわかってきた。AREまたはGPE Iの配列を介した第2相の薬物代謝酵素に共通の誘導機構が存在するのではないかと推測される。AREや GPE Iの配列はXREの配列とは全く異なり,第2相の薬物代謝酵素の誘導機構にはAh 受容体を介する機構とは別の機構が存在することも考えられる。GST-Pはまたある種の細胞増殖因子によっても誘導され,この誘導にもGPE Iの配列が関与しているという結果が得られている。
コプラナーPCBなどのように癌化を促進する作用のある物質や増殖作用を持つ物質と癌化に結びつく酸化ストレスを防御する作用を持つ物質が同じような機構で第2相の薬物代謝酵素を誘導するというのは不思議である。コプラナーPCBの癌化促進作用とGST-Pなどの薬物代謝酵素の誘導発現の関係について追求してみたいと考えている。
執筆者プロフィール:
大阪府出身,京都大学薬学部卒。


