藻類の多様性研究と種判別法の開発
-ピコ植物プランクトンを例に-
●特集 DNAを通して自然を観る●
【シリーズ重点研究プログラムの紹介:「生物多様性研究プログラム」から】
河地 正伸
藻類の多くは単細胞性で、形態的な特徴はそれ程多いとはいえません。種の分類・同定には、いろいろな顕微鏡的な形質を組み合わせることで行っていて、専門的な知識と経験が必要です。また、形に頼らずに種の識別が可能なDNAバーコーディング情報(「環境問題基礎知識」参照)は、残念ながら藻類ではほとんど整備されていないのが現状です。
2011年度から始まった生物多様性研究プログラムでは、プロジェクト-1「生物多様性の景観的および遺伝的側面とその観測手法に関する研究」において、ピコ植物プランクトン、霞ヶ浦の藻類、そしてサンゴに共生する褐虫藻などを対象として、多様性研究や種判別法の開発を行っています。培養や観察が困難な藻類の実態を種レベルで解明するために環境DNA(様々な微生物由来のDNAが混在する試料)中のゲノム情報の収集とその解析結果に基づく多様性研究を進めるとともに、培養できる種については、DNA配列から種同定が行えるように種の情報とDNA情報の収集・整備を進めています。更にこうして集積した情報に基づいて、より簡便な種判別法や定量的なモニタリングを行うための手法開発にも取り組んでいます。ここでは、ピコ植物プランクトンを中心に、これまでの研究成果について紹介したいと思います。
ピコ植物プランクトンは、細胞サイズが2μm以下(1μmは1/1000mm)の微小サイズの植物プランクトンで、水環境に広く生息しています。特に外洋環境などの貧栄養環境では、優占的に存在して、窒素循環や炭素循環に大きく寄与することが知られています。一方で、大量増殖して生態系の高次消費者を含む他の構成生物に大きく影響を及ぼしたり、オゾン層破壊に関与するハロゲンガスを産生したりすることで問題視されることがあります。既存の種類として、約30種程が知られているだけですが、最近の環境DNAの解析からは、ピコ植物プランクトンには、既存の種より遙かに多様で、新規な分類群が多数存在することが示唆されています。ここでピコ植物プランクトンに関わる研究の課題について少し整理してみたいと思います。
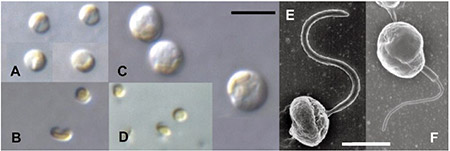
まず挙げられるのは、細胞サイズの微小さと形態の単純さです。多くのピコ植物プランクトンは、球形、楕円形などの単純な形態をしていて(図1)、種の同定には、電子顕微鏡による微細構造の観察やDNA情報の解析が必要です。こうした詳細な観察、解析には培養株が必須なのですが、バクテリアサイズの細胞を培養のために顕微鏡下で分離するのは困難を伴う作業です。複数の種が混ざっている場合、それらを区別して分離・培養するのはほとんど不可能です。環境適応力が高く、増殖の早い種だけが培養株として確立されてくることになります。その結果として、ごく限られたピコ植物プランクトンだけがこれまで研究対象とされてきました。
次に挙げられるのは培養の困難さです。貧栄養な外洋環境や有光層最下層などの低照度条件によく適応した種では、実験室で再現した培養条件下ではなかなか増殖できないのが現状です。他にも課題はありますが、これら2点がピコ植物プランクトンの研究遅延のボトルネックになっています。
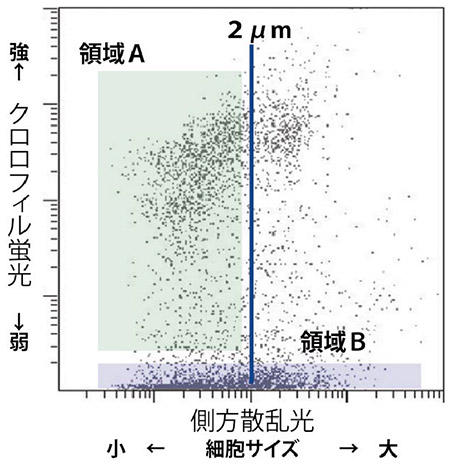
2012年7月に仙台湾表層で採取した海水中の細胞を約100倍に濃縮して、細胞分取機能付きのフローサイトメトリという細胞解析装置で解析した像を図2に示します。1秒間に1万もの細胞を解析することが可能です。縦軸はクロロフィルの蛍光値、横軸は細胞サイズと相関する側方散乱光の値、グラフ内の1つ1つの点は、フローサイトメトリで検出された1個1個の細胞になります。中央に記した縦線より左側には2μm以下の細胞が多く含まれています。バクテリアや従属栄養性の原生動物のようなクロロフィル蛍光のない細胞は横軸に沿って分布しています(図2の領域B)。領域Aには細胞サイズが2μm以下で、クロロフィルの蛍光をもつ細胞が多く含まれることになります。海水中の全細胞を対象として、遺伝子解析を行うと、領域Bに含まれるような非光合成(寄生性、従属栄養性)の生物が40-80%を占めることがあります。一方、クロロフィル蛍光をもつ細胞を同装置で分取すると、大部分が光合成生物となります。効率よくピコ植物プランクトンを解析するのに、フローサイトメトリは有効な手段と言えます。
このフローサイトメトリを用いてピコ植物プランクトンを含む領域から細胞を分取して、膨大なDNA情報を一度に取得可能な次世代シーケンサーを用いて、種判別に有効な特定遺伝子領域のDNA情報を取得しています。こうしたDNA情報を基に、種同定や類似配列の出現頻度の解析を行うことで、どのような生物が優占的に存在していたのかを推定できるようになります。結果の詳細は省略しますが、仙台湾の7月の試料の場合、優占種と思われる配列のうち、属レベル以下で同定できたのは僅か15%程度で、残りはWeb上で公開されている塩基配列データベースに“難培養性真核生物”や“未知真核生物”として登録されているいろいろな配列に辛うじてヒットするような配列でした。一部、培養株で登録された配列と同じ配列も見つかっていますが、大部分は多様な系統群で構成される新規な配列になります。フローサイトメトリで分取した細胞は培養に利用することも可能です。分取する領域を細かく設定するなどして、優占種の培養に取り組むことで、新種を含む様々なピコプランクトンの培養株が得られるだろうと期待しています。ピコ植物プランクトンの実態を明らかにするための重要なステップです。
国立環境研究所の微生物系統保存施設では15種あまりのピコ植物プランクトン保存株が維持されています。こうした保存株や今回のプログラムで新たに確立した培養株について詳しく遺伝子解析することで、種判別に有効なDNA情報の収集やT-RFLP法(末端標識制限酵素断片多型分析法)を用いた簡便な種判別法の開発にも取り組んでいます。また培養株を用いた実験から、細胞構造が比較的単純なピコ植物プランクトンは、生きたまま容易に凍結保存できることが分かってきました。ピコ植物プランクトンを多く含む環境試料を液体窒素の中で凍結保存しておくことで、繰り返し、再現性の高い実験が可能となります。フィールドで採取した試料を一旦凍結保存しておいて、そこからフローサイトメトリで特定の細胞集団を分取してまずDNA解析を行います。もしも新規で面白いピコ植物プランクトンが見つかれば、より詳細な解析や培養を行うために、凍結保存しておいた試料を解凍して、繰り返し細胞を分取、解析に用いることも可能です。こうしたストラテジーで、現在研究を進めています。
執筆者プロフィール

DNAというものさしを使って調べた微生物の多様さは、陸上植物や後生動物を遙かに凌駕するものです。次世代シーケンサーが普通に使われ始めた昨今、微生物多様性の研究分野で、nature級の発見が相次いでいます。一方、実在の生物を、DNA情報だけで解析することの限界も見え始めていて、培養技術や保存株の重要性を再認識しているところです。






