有毒アオコをめぐる研究の動向
研究をめぐって
有毒アオコによる事故は1920 年代から報告されていましたが、1980 年代になりアオコの有毒物質の構造が決定されました。1998 年には世界保健機構(WHO)により飲料水中のミクロシスチンについて暫定的な基準値が勧告されました。また、アオコの増殖を抑制する技術や、ミクロシスチン等のアオコの有毒物質の除去・分解方法についても検討されています。

世界では
1980年代からアオコの有毒物質であるミクロシスチン、シリンドロスパーモプシン等の構造解析が行われていて、現在では100種類以上のミクロシスチン同族体が報告されています。高速液体クロマトグラフ-タンデム型質量分析計(LC-MS/MS)を用いたミクロシスチン同族体の個別分析手法についても早くから検討されていて、定量だけでなく構造解析もLCMS/MSで行われてきました。
WHOでは、1996年に起きたブラジルでのヒトの死亡事故をうけて、1998年にミクロシスチン-LRの暫定基準値(1μg/L)を勧告しました。この勧告を受けて、ヨーロッパの国やオーストラリアではミクロシスチンの基準値を定めて、厳しく監視しています。また、水酸化カルシウムを用いたリン酸の除去手法や、過酸化水素や草食魚等を用いたアオコの増殖抑制手法などの検討が行われています。
日本では
1980年代後半にアジア地域で量が多いミクロシスチン-RRの構造解析が筑波大学の楠見武徳博士らにより報告された後、多くの同族体の構造が日本人研究者により報告されてきました。日本のアオコは欧米のアオコと比較して毒性が弱いものが多く、健康被害や家畜の斃死などは記録されていませんが、日本各地の富栄養化が進んだ湖沼で有毒アオコの発生が確認されています。
アオコの有毒物質の中ではミクロシスチンが最も高頻度で確認されていて、環境省では平成10年に要調査項目、厚生労働省では要検討項目や上水試験法の試験項目に指定していますが、基準値にはなっていません。また、ミクロシスチンやシリンドロスパーモプシン等の有毒物質を合成する酵素の遺伝子やミクロシスチンを分解する酵素の遺伝子等を調べることにより、環境中での有毒アオコやミクロシスチンの動態などについても研究が進められています。
国立環境研究所では
生物系や工学系の研究者たちは、1980年代から藍藻類の分類や増殖条件、ミクロシスチンの産生条件の検討、水生生物によるミクロシスチンの濃縮などについて研究を行っていて、「アオコの見た目指標」なども作成しました。最近では遺伝子解析による分類や有毒株の判定、分化の推定などについても研究しています。また、富栄養化の原因となる栄養塩類の推移やアオコの増殖抑制、生物膜処理によるミクロシスチンの分解等についても研究を行っています。
化学系の研究者は、有毒物質の構造解析としては、1995年にDhb-ミクロシスチンの発見、1996年には魚類に毒性を示すチオンスルホフォリピドの単離、2011年には環境ホルモン作用のある7-ヒドロキシレチノイン酸の単離などを行っています。
毒性の評価法の開発としては、1996年にはエレクトロポレーションによる細胞毒性評価手法の開発、2010年にはトロピカルテクノセンターとの共同研究で遺伝子組み換え蛋白質脱リン酸化酵素(PP2A)を利用したマイクロプレートアッセイ法の開発、2011年には国立医薬品食品衛生研究所との共同研究で凍結初代培養幹細胞を用いた毒性評価システムの開発などを行ってきました(表3)。
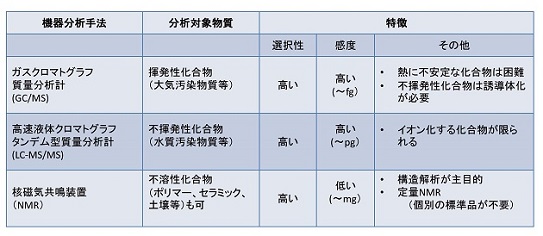
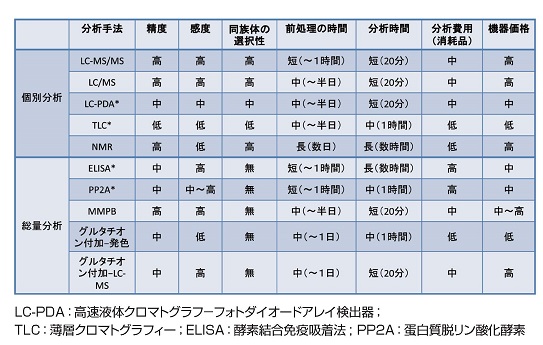
個別分析法では、LC-MS/MS法が感度・精度・選択性・迅速性全てで優れていますが、分析機器が高額です。NMRは感度が低いので、低濃度の分析は現実的ではありません。
総量分析法では、ELISA法は感度は高いのですが精度が高くなく、キットも高額です。グルタチオン付加-発色法は精度は良くないですがコストが安く、高額な機器を必要としないことから、開発途上国でも使いやすい分析法と思われます。
(測定値のばらつきが小さいと精度が高い、微量で測定できると感度が高い、同族体を区別できると選択性が高いと表示しています。)
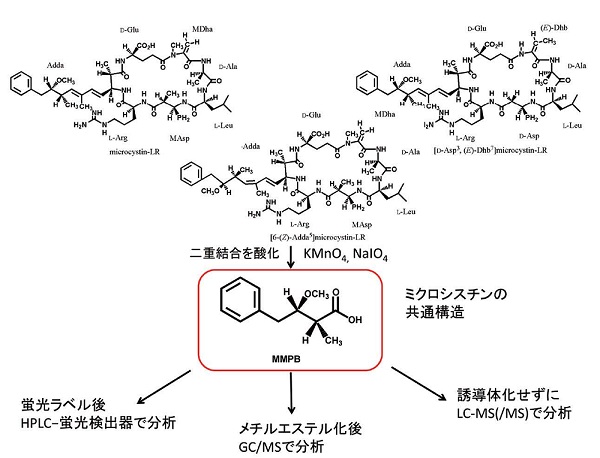
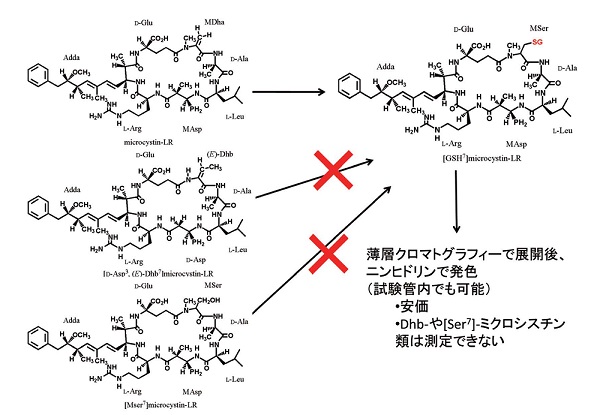
分析法としては、1992年にミクロシスチン総量分析手法であるMMPB法を開発(図4)、2001年には、高額な分析機器を持たない開発途上国でも分析ができるように、ミクロシスチンにグルタチオンを付加させて安価に分析する方法の開発も行いました(図5)。
2005年には研究者が自分の分析の確からしさを確認できるようにするために、ミクロシスチン分析用の環境標準物質(NIES CRM No.26アオコ)を開発しました(図6)。2010年には安定同位体標識ミクロシスチンの調製と高精度分析手法の開発などを行ってきました。

環境試料は化学組成が極めて複雑なため、試料の前処理や測定が難しく、単純な標準溶液を用いたのではなかなか正しい分析値を求めることができません。このような場合には、分析試料と化学組成がよく似た標準物質を用いることにより、分析値の正確さを向上させることができます。
アオコの有毒物質ミクロシスチンの分析精度管理用の環境標準物質を作製するために、有毒な藍藻株を大量に培養し、凍結乾燥しました。乾燥藻体を混ぜ合わせ、63μmのふるいを通しました。この細かい粉体をビンに小分けした後、均質性試験、認証値付与、安定性試験を行い、環境標準物質(NIES CRM NO.26アオコ)が完成しました。NIES CRM NO.26は、ミクロシスチンの分析用に開発された環境標準物質です。
また、ミクロシスチン以外で高頻度で検出される有毒物質シリンドロスパーモプシンについても、種類の異なる固相抽出カートリッジを連結して使用することにより、簡便に濃縮する手法の開発や、安定同位体(15N)で標識されたシリンドロスパーモプシンの調製と、それを用いた高精度分析手法の開発も行ってきました。
人為的な環境汚染物質による汚染とは異なり、アオコ発生の主な原因は富栄養化であるためにアオコの制御は難しく、今後も地球温暖化の進行に伴い、世界中で有毒アオコの発生が問題になると考えられています。有毒アオコによる被害を抑制するためには、アオコの発生を抑制する技術の開発とともに、ミクロシスチン等の有毒物質を注意深く監視していく必要があります。今後もアオコの有毒物質の構造解析や、アオコの有毒物質に対する迅速・簡便・高精度な分析手法の開発がますます重要になると考えています。