ヒト組織由来細胞を用いて、化学物質の神経発達への影響を明らかにする
Summary
これまで、ホルモンが関連するがんや生殖器の発達不全、神経発達障害などの病態において、環境化学物質がどのように関与するのかを明らかにするための基盤研究を行ってきました。研究の成果は、正確な化学物質のリスク情報を提供し、人々が健康で安全な生活を営むための予防策の策定に貢献しています。
ダイオキシンおよび内分泌かく乱化学物質による健康影響における毒性経路の解明
1998年から2001年にかけて、ダイオキシンおよび内分泌かく乱化学物質による健康影響が社会的にクローズアップされました。その際、核内受容体に作用して転写を活性化させ、下流の遺伝子群の発現に影響を及ぼして生体影響を示す化学物質、いわゆる「核内受容体作動性化学物質」の存在が科学的に認知され、それらの有害性を確認することが重要だと認識されるようになりました。
これより少し前の1996年にロンドンで第1回内分泌かく乱化学物質の健康と野性生物への影響に関するヨーロッパワークショップが開催され、男性の精子数の減少や性ホルモンに関連した乳がん、前立腺がん、卵巣疾患などの発症の増加との関連が指摘されていました。それまで、動物実験が中心だった研究が、ヒトの健康における生殖と発生への影響を調べるために、性ホルモン受容体、それに関わる細胞周期、増殖への影響を調べる研究へ移行しました。ヒト子宮内膜がん細胞、乳がん細胞、前立腺がん細胞、胎盤絨毛がん細胞などを用いて、女性ホルモン受容体や男性ホルモン受容体の存在量に応じて、低濃度のダイオキシンの曝露によって誘導される薬物代謝酵素遺伝子の発現量、細胞が分裂増殖を継続し続ける性質に関与しているタンパク質や、過剰発現するとがんを引き起こすことが知られているがん遺伝子の発現が変化することを明らかにしました。
また、生物の発生段階から成熟体の恒常性維持・疾病など多彩な生体プロセスの制御に強く関与する因子が女性ホルモンによって制御されていることを示しました。正常および患者由来皮膚細胞や乳がん細胞に、ビスフェノールA(BPA)を曝露すると、特異的に応答する遺伝子は、細胞ごとに異なりました。特に、停留精巣や尿道下裂の患者由来の皮膚の線維芽細胞を用いた研究では、皮膚の支持基盤を構成する分子が選択的にBPA曝露により抑制されることがわかり、その抑制の強さには、個人差があることがわかりました。
ヒトES細胞を用いた有害物質の曝露による神経発達影響のメカニズムの予測
DOHaD(developmental origins of health and disease)仮説では、胎児期と出産後の初期の発達時期の環境状況が成長、体躯や臓器の構造と代謝に対する影響を通して生涯の健康と能力に影響すると、提唱されています。この事象はプログラミングと呼ばれています。初期発生を含む胎生期の全過程では、時期特異的な遺伝子やタンパク質の発現が入れ替わり、胎児期のプログラミングを整えていきます。この胎生期プログラミングの分子メカニズムは、DNAのメチル化修飾や染色体のヒストンタンパク質のアセチル化修飾などによる遺伝子発現制御が基盤となっています。その過程を模倣するモデル細胞として、ヒトES細胞に着目し、未分化や分化初期の化学物質曝露がその後に現れる晩発影響を調べました。
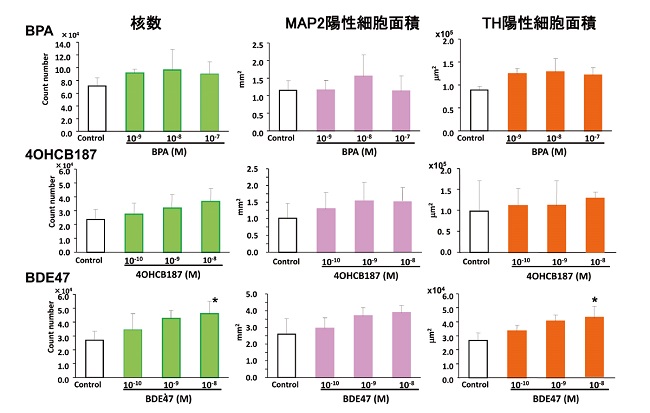
メチル水銀に対するヒトとマウスの感受性を比較した研究では、神経細胞の突起伸長に対してヒトES細胞は、マウス ES細胞よりもメチル水銀の感受性が高く、神経分化に関与する遺伝子群への影響もより強いことを明らかにしました。さらに、同様に、ヒトES細胞を用いて、ヒトで催奇形性を引き起こすことが知られているサリドマイド、疫学調査や動物実験から神経発達障害への関与が懸念されているPCB代謝物である水酸化PCB、難燃剤BDEおよびBPAの神経細胞への分化の影響を調べたところ、難燃剤BDEでは、神経突起の伸長を抑制しました(図5)。炎症や神経のシグナル伝達に関与する遺伝子群も変動していました。これらのことから、小児の神経発達に影響を及ぼす潜在的な能力があることが考えられます。
ヒト神経前駆細胞の3次元培養における新たな環境有害要因による影響
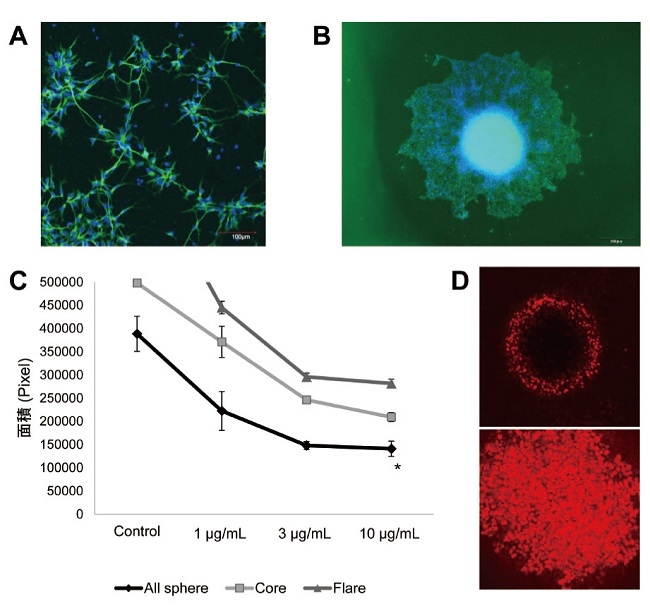
ヒトES細胞から成熟した神経細胞までには長い道のりがあり、神経幹細胞を経てヒト神経前駆細胞が生まれます(コラム1図1)。ヒト神経前駆細胞を用いて、放射性セシウムやナノマテリアルの曝露の影響を調べました。細胞の機能を高く維持することが可能な3次元培養法を用いて、より生体内に近い状態で実験を行いました。3次元培養で作成したヒト神経前駆細胞のスフィア(細胞塊)に、放射性セシウムを照射した実験では、これまでの報告よりも低い線量でDNA傷害や炎症性遺伝子が誘導されることがわかりました。神経突起の伸長などが線量依存的に抑制されることもわかりました。また、デンドリマーという薬物輸送に用いられる樹状ナノマテリアルの曝露による影響を調べた研究では、デンドリマーの大きさや表面の電荷の状態によって、神経突起の伸長や神経細胞への分化が変化することがわかりました(図6)。
このように、有害化学物質の発達への影響のメカニズムをよりよく理解するためには、ES細胞や組織における幹細胞を用いた研究が今後も必要です。
目次
-
 化学物質の正確なヒト健康への影響評価を目指して -新しい発達神経毒性試験法の開発-環境儀 No.65
化学物質の正確なヒト健康への影響評価を目指して -新しい発達神経毒性試験法の開発-環境儀 No.65
-
 ES細胞を用いて、化学物質のヒトへの影響を予測するInterview研究者に聞く
ES細胞を用いて、化学物質のヒトへの影響を予測するInterview研究者に聞く
-
 多能性幹細胞を用いて胎児期の影響を調べるコラム1
多能性幹細胞を用いて胎児期の影響を調べるコラム1
-
 ヒトの健康影響を調べるためのインビトロとインビボ試験の有用性と問題点の比較
ヒトの健康影響を調べるためのインビトロとインビボ試験の有用性と問題点の比較
コラム2 -
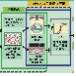 化学物質の健康影響評価の変革コラム3
化学物質の健康影響評価の変革コラム3
-
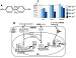 内分泌かく乱化学物質ビスフェノールAの健康への影響:種差はあるのか?コラム4
内分泌かく乱化学物質ビスフェノールAの健康への影響:種差はあるのか?コラム4
-
 ヒト組織由来の細胞、ES/iPS細胞を用いた化学物質が健康に及ぼす影響の予測法研究をめぐって
ヒト組織由来の細胞、ES/iPS細胞を用いた化学物質が健康に及ぼす影響の予測法研究をめぐって
-
 国立環境研究所における「ヒト細胞を用いた発達神経毒性試験法と発達期影響予測法の開発に関する研究」のあゆみ
国立環境研究所における「ヒト細胞を用いた発達神経毒性試験法と発達期影響予測法の開発に関する研究」のあゆみ
-
 過去の環境儀から
過去の環境儀から
-
 PDFファイル環境儀 NO.65 [3.34MB]
PDFファイル環境儀 NO.65 [3.34MB]
目次
- 化学物質の正確なヒト健康への影響評価を目指して -新しい発達神経毒性試験法の開発-環境儀 No.65
- ES細胞を用いて、化学物質のヒトへの影響を予測するInterview研究者に聞く
- 多能性幹細胞を用いて胎児期の影響を調べるコラム1
-
ヒトの健康影響を調べるためのインビトロとインビボ試験の有用性と問題点の比較
コラム2 - 化学物質の健康影響評価の変革コラム3
- 内分泌かく乱化学物質ビスフェノールAの健康への影響:種差はあるのか?コラム4
- ヒト組織由来の細胞、ES/iPS細胞を用いた化学物質が健康に及ぼす影響の予測法研究をめぐって
- 国立環境研究所における「ヒト細胞を用いた発達神経毒性試験法と発達期影響予測法の開発に関する研究」のあゆみ
- 過去の環境儀から
- PDFファイル環境儀 NO.65 [3.34MB]