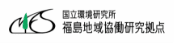除去土壌の中のセシウム
福島第一原子力発電所事故により東日本の広い範囲が放射性セシウムにより汚染され、その後、帰還困難区域を除く地域の除染は終了し、2021年度中にはすべての除去土壌が中間貯蔵施設に搬入され、2045年までに再生利用と福島県外での最終処分が実施されることになっています。
空から降下した放射性セシウムはあらゆるものに付着しました。
除染のために屋根を洗浄し、住居近傍の植生を除去し、さらには地表の土壌を除去しました。
これらの除染により環境中の放射性セシウムによる線量率は低下しました。

放射性セシウムの移動については、土壌から植物が一部吸収し人の手で移動したり、水害により河川水系で土壌ごと流下したり、土中の生物がかく乱したりするということはありますが、土壌から放射性セシウムが溶け出して環境に検出できるほど拡散するということはありませんでした。
このように事故により飛散した放射性セシウムが土壌の表層にとどまっていたがゆえに、表層土壌を除去することで除染が可能でした。
ではなぜ放射性セシウムは土壌から動かなかったのでしょうか?
今回は、土壌とセシウムの相互作用の本質を考えてみます。
フレイドエッジサイト
土壌中で放射性セシウムを特に吸着する物質は黒雲母という鉱物が風化して生成するヴァーミキュライトであることが分かっています。
このヴァーミキュライトはシリカ(SiO2)とアルミナ(Al2O3)を主成分とし、金属イオンとして、マグネシウム、鉄、カリウムを含有する層状化合物で粘土鉱物の一種です。
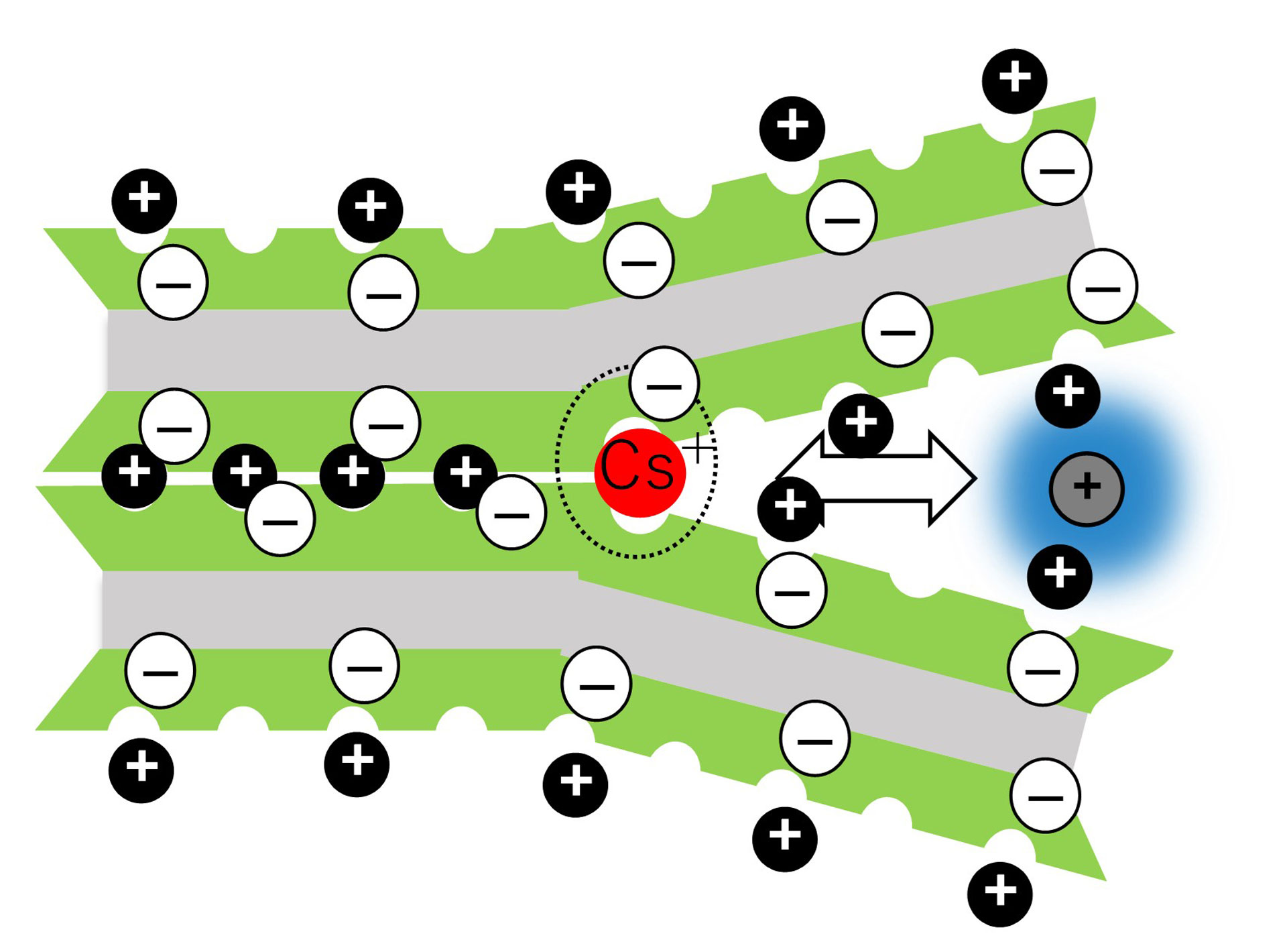
図1 ヴァーミキュライトのフレイドエッジサイトでのCs(赤)の特異吸着(文献1を編集)
図1の緑色がシリカの層で、灰色がアルミナの層です。
シリカの層の一部をアルミナが置き換えると、Siが4+でAlが3+であり、SiもAlも同数の酸素4個に取り囲まれる構造となっているため、その置換部位では正電荷が1個足りなくなり、層状粘土鉱物の層間の表面は負に帯電することになります。
この負電荷の位置に、陽イオンを吸着する性質が生まれます。
自然界では、正負の電荷は必ず中和しているので、この陽イオンを吸着するサイトには必ず何らかの陽イオンが存在しています(図1の黒丸)。
1荷の陽イオンが吸着しますが、その吸着しやすさは実験するとNH4+>Cs+>Rb+>K+>Na+になります。
また、ヴァーミキュライトの層状構造の端部は、図1の右側のように膨潤し開いていてフレイドエッジサイトと呼ばれています。
このフレイドエッジサイトの寸法がセシウムのイオン半径とぴったり一致するから、強い吸着が起きると説明されています1)。
セシウムが特に吸着されやすいという説明です。
直感的にとても分かりやすい説明です。
ですが、実はその奥に深い理由があるのです。

原石バーミキュライト(ホームセンターなどで販売されている保水性の園芸土は焼成されたヴァーミキュライトであり、焼成によりセシウム吸着特性はほとんど無くなっています)。
イオン交換体
層状粘土鉱物は陽イオン吸着能を持つわけですが、この吸着は活性炭が極性を持たない臭いの分子などを吸着する現象とは異なる原理で吸着されます。
層状粘土鉱物の吸着サイトには、必ず1荷の陽イオンが存在し、それが別のイオンと交換するだけです。
セシウムイオンが来ると、もとあったカリウムイオンが追い出されて、セシウムが「吸着」されます。
なので、この現象は吸着ではなく、イオン交換と呼ばれるべきものです。
そして、層状粘土鉱物はイオン交換体としてはたらきます。
その吸着サイトとイオンの結合は実は強いものではなく、溶液中のイオンと簡単に交換できるものです。
個別のイオンに名前を付けるとして、セシウム1番さんが先に席(吸着サイト)についていて、あとからセシウム2番さんがやってくると、一定の確率で置き換わります。
活性炭が電荷をもたない臭いの分子を分子間力と呼ばれる相互作用で表面に居座るような形で吸着するのとは仕組みが違います。
この席をめぐっては、溶液に存在する各種の陽イオンがその席をめぐって競争します。
直感的には、席についた状態で安定なイオンが席に着きそうなものです。
イオン一つずつを見るとカリウムよりもセシウムが付きやすいとしても、セシウムの数に比べ、カリウムの数が多いと、セシウムが席につける確率は小さくなるのです。
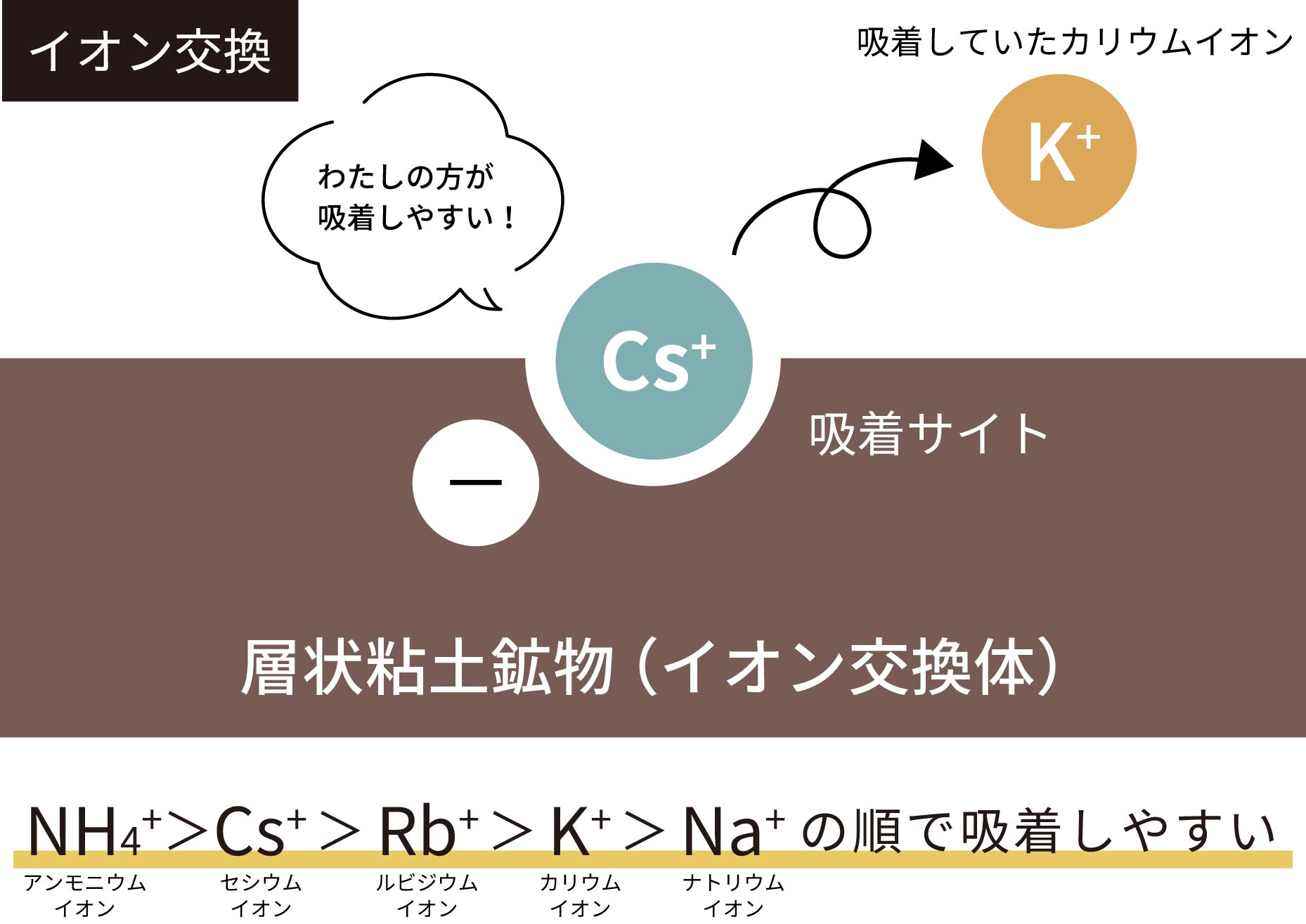
地殻中にはカリウムは23,000ppm、セシウムは3ppm存在するので、濃度比は約7,000です。
海水中では、カリウムは400ppm、セシウムは0.0003ppm(300ppt)存在するので、濃度比は約1,300,000となります。
地殻と海水での濃度比の違いを水への溶けやすさの違いだと考えると、セシウムはカリウムよりも約200倍溶けにくいことになり、それだけセシウムは地殻の構成鉱物に取り込まれやすいことになります。
より詳しく書いてみます。
雨水は、海水を巻き上げ水蒸気とともに雨粒となって地表に降下したものです。
したがって、雨水中のカリウムとセシウムの濃度比は海水と同じと考えられます。
雨水中のカリウム濃度は推定例があり0.13ppmですので、同じ比だと考えるとセシウム濃度は100ppq(ppmの10億分の1)となります。
事故で放出されたセシウムの雨水中での濃度をいくつかの仮定を設けて計算すると130ppt(ppmの100万分の1)となり、雨水よりも1000倍濃いことになります。
通常、土壌は雨水にさらされていて、かなり薄いセシウムと接触してきたのですが、事故後は1000倍ほど濃いセシウムに接触したために、事故によりもたらされた放射性セシウムのほとんどが土壌に吸着したと推定されます。
なぜセシウムが一番吸着されやすいのか?
次に、セシウムがどうしてほかのナトリウムやカリウムよりも吸着されやすいのかを説明します。
フレイドエッジサイトでは寸法がマッチするから、という説明をしましたが、実はもう少し複雑です。
図2にイオン交換体の一種であるセメント水和物(ケイ酸カルシウム水和物)表面へのセシウムとナトリウムの共存状態での吸着状況を示します。
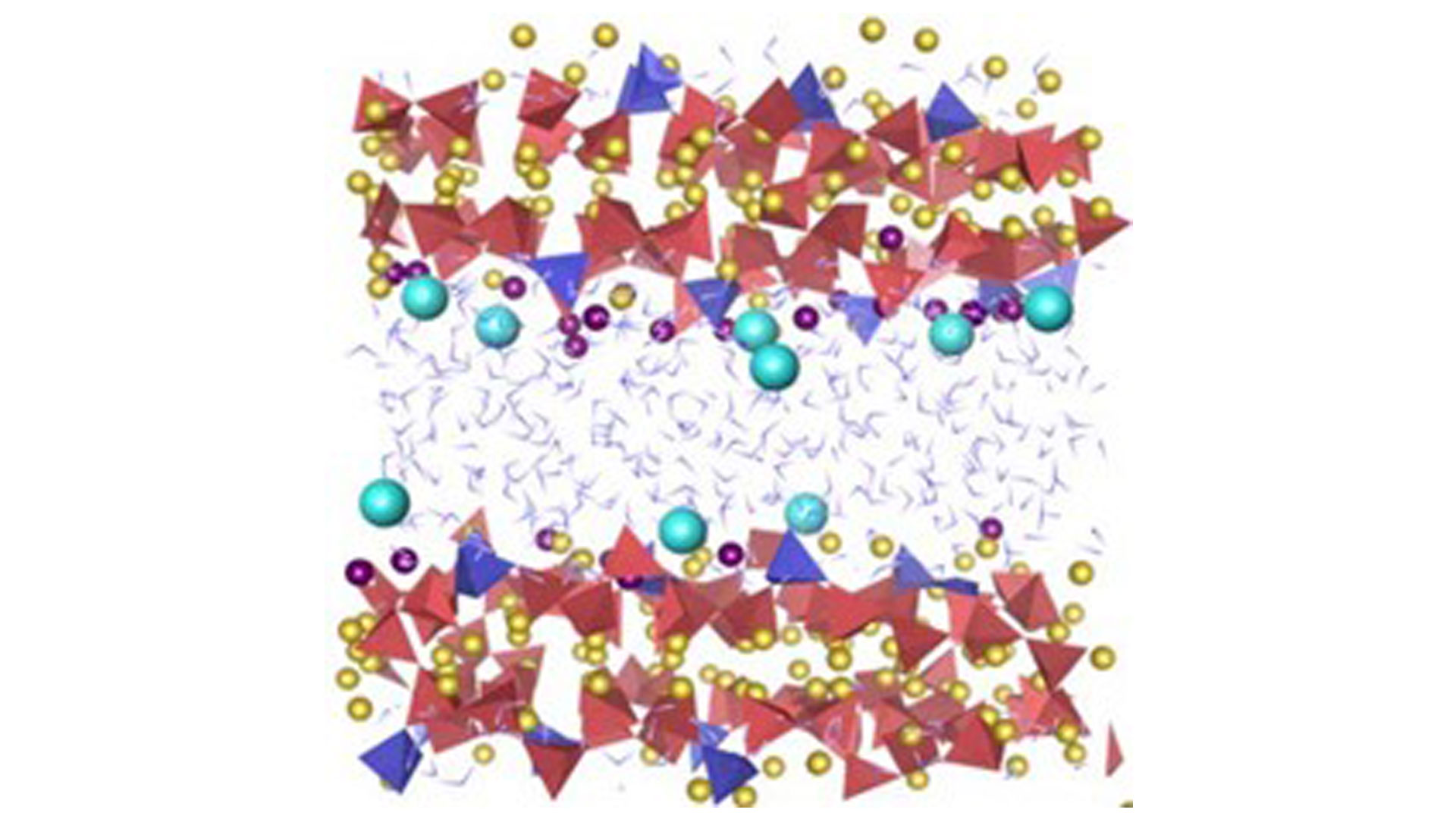
図2 セメント水和物表面でのセシウム(水色)とナトリウム(紫)の吸着状態の分子動力学シミュレーション2)
イオンの大きさはNa<Csですので、静電力で結合していることから、距離が近くなるナトリウムの方が安定です。
セシウムが一番吸着しやすいという説明と矛盾します。
計算が間違っているのでしょうか?
これは吸着を、吸着後の姿だけで考えるためです。
吸着反応に係る内容を図3に示します。
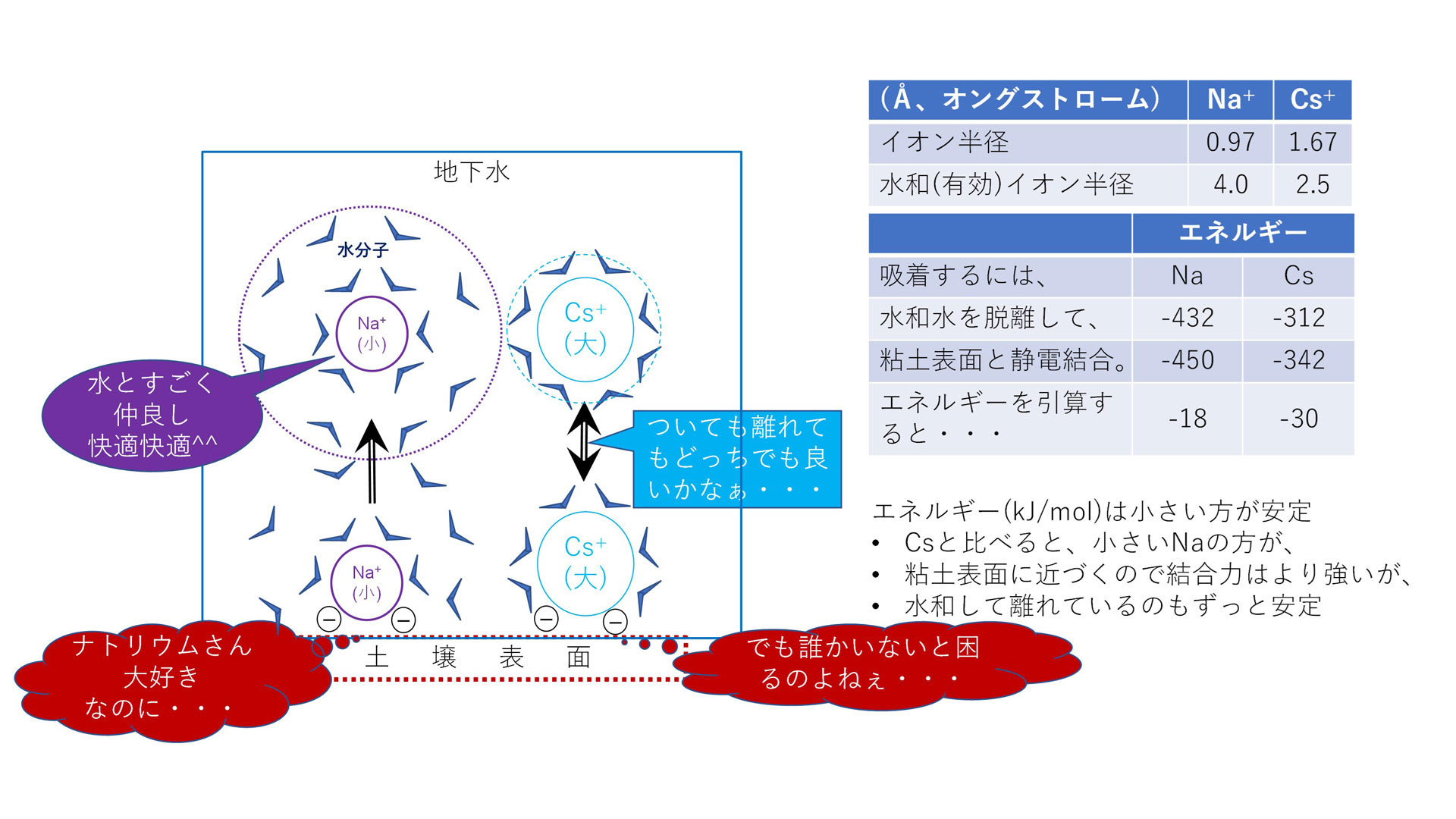
図3 吸着前後のエネルギー差を考えたナトリウムとセシウムの吸着しやすさ
吸着は水溶液中の水和したイオンが部分的に水和水を離しながら吸着します。
ということは、吸着しやすさだけではなく、水和水との離れやすさも考えないといけないことになります。
ナトリウムとセシウムを比較して説明します。
ナトリウムは吸着によるエネルギーの安定化はより大きいのですが、水和エネルギーもより大きいのです。
吸着は部分的に水和水を離して起きます。
図3の例では水2分子を離しています。
図1の場合はより多くの水和水分子を離して吸着します。
このように吸着は水和状態から吸着状態へのエネルギー変化を考えないといけません。
差を取ってみるとセシウムの方がより安定であることが分かります。
これが吸着しやすさの序列が発生する原理です。
そして、吸着状態が水和水をどれだけ許容できるかで、セシウムと他のイオンとの選択性が決定します。
水分子を全く許容しないプルシアンブルーなどセシウムの吸着剤は極めて高いセシウム選択性(1万程度)を示しますが、部分水和した形で吸着する粘土のセシウム選択性は10程度とかなり低くなります。
土壌からセシウムはなぜ出てこないのか?
ここまで、粘土はイオン交換体で吸着されたイオンは外界のイオンと交換する、と説明しました。
地下水にセシウムは微量ながら含まれているのですから、そのセシウムイオンと交換し、少しずつ環境にセシウムは漏れ出しても不思議ではありません。
汚染した現実の土壌を、高濃度のセシウムイオン、もしくはアンモニウムイオンを含む水溶液に浸漬しても、95%の放射性セシウムは溶けだしてきませんでした。
これはなぜでしょうか?
イオン交換による吸着速度には、イオン交換の速度も関係します。
図3のような開放面であればイオン交換は速やかに起きます。
しかし、図1のような場合は、フレイドエッジ先端の位置に吸着された後、一つ奥の吸着サイトに移動するのに時間を要します。
奥にあるカリウムよりもセシウムを吸着したほうが安定なので、熱振動でゆっくりと交換反応が進んでいきます。
いったん奥に入ってしまうと、今度はそう簡単には環境に放出されなくなると考えると、土壌からセシウムが出にくいことを説明できそうです。
あるいは吸着後に、フレイドエッジが閉じてしまったり、粘土鉱物自体が溶解再沈殿したりてもセシウムは出にくくなるでしょう。
つまり、はじめはイオン交換性のセシウムとしてとらえられたものが、時間の経過とともに非イオン交換性のものに変化したと考えられます。
なお、いずれの場合においても、セシウムはカリウムに対して圧倒的に少量であるので、セシウムを主体とする鉱物が生成するとは考えにくく、カリウムを主成分とする鉱物のごく一部のカリウムを置き換えてセシウムは存在するはずです。
このように安定に吸着するのに時間がかかるのでは、セシウムを水溶液から選択的に吸収する吸着剤には向きませんが、環境においては時間がたつほど強固に吸着するので好都合と言えます。
あわせて読みたい
参考文献
- 山口紀子(2014)土壌への放射性Csの吸着メカニズム.土壌の物理性, 126, 11-21
- Duque-Redondo E, Yamada K, Dolado JS, Manzano H (2021) Microscopic mechanism of radionuclide Cs retention in Al containing C-S-H nanopores. Computational Materials Science, 190, 110312
- 市川恒樹、山田一夫、芳賀和子(2022) 解説セシウム吸着剤を用いた放射性セシウム汚染廃棄物の超減容化処理 -イオン交換体とイオン交換反応-、環境放射能除染学会誌(印刷中)