はじめに
産着卵の分布調査を行う理由
琵琶湖に生息するコイ・フナ・ホンモロコ類は、本湖固有の魚種を含んでおり、生物多様性の観点から貴重な魚たちです。フナ寿司などの伝統的な食文化を支える食材でもありますが、その漁獲量は1980-90年代以降激減して現在に至っています。主な原因としては、外来魚の蔓延や産卵場所の土地改変、人為的な琵琶湖の水位調節などがあります( 藤岡 2013; 馬渕, 松崎 2017)。琵琶湖分室では、劣化・消失した産卵場所を適切に保全・再生するため、各魚種の現在の産卵場所を正確に把握する調査を行っています。詳しくは「在来コイ科魚類の産着卵調査」をご覧ください。
産着卵分布の調査方法
琵琶湖のコイ・フナ・ホンモロコ類の多くは、沖合の深場で冬を越しますが、春になると湖岸や流入河川・水路に移動し、水辺の植物や浮遊物等に卵を産み付けます(図1)。産着卵の分布調査は、このような場所において、目視で産み付けられた卵(産着卵)を探索することにより行われます。滋賀県が定める保護水面における卵の採集は、特別採捕許可を得て行っています。




調査区域内で卵を見つけたら、例えば同じ葉に産み付けられている近接した卵10-30個ほどを一つの「卵群」として採集し、同時に、採集した地点の緯度経度をGPS端末で記録します。卵が見つからなかった場所についても同様に緯度経度を記録します。採集した各卵群にはGを冠した固有の番号(例えばG1129やG2445:図2)を振り、対応する採集地点や採集年月日等の情報と紐付けします。卵が見つからなかった場所の緯度経度の情報も探索年月日と紐付けしておきます。


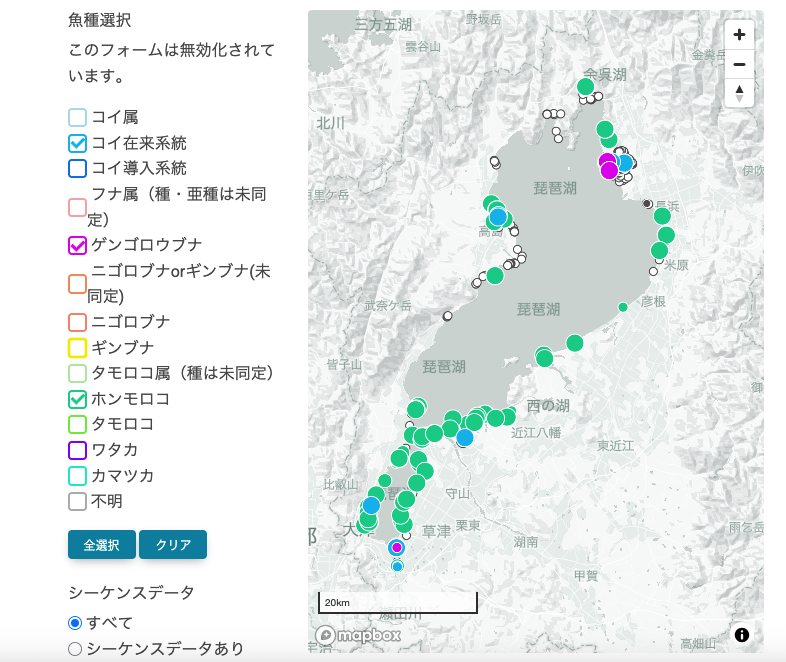
実験室に持ち帰った卵群は、エタノールで固定してマイナス20度からマイナス30度で保存します。後日のDNA解析では、一つの卵群から基本的に8個の卵をランダムに選び、卵1個ずつからDNAを抽出し、それぞれについて魚種を同定します。各卵の種が同定できたら、その結果を地図上の採集地点にプロットし、どの魚種の卵が(いつ)どこに分布していたかを可視化します(図3)
産着卵のDNA種判別
基本的にミトコンドリアDNAを解析対象とし、卵の産着状況によって2つの方法を使い分けています。
- (a)
- 水面近くの植物体や浮遊物等に高い密度で付着している卵 PCRの増幅断片(ミトコンドリアDNA及び核マイクロサテライト領域)の長さによる種判別
- (b)
- 上記以外の卵 部分塩基配列の決定による種判別
ほとんどの卵は前者による種判別を行いました。それぞれの詳細は以下の通りです。
(a) PCRの増幅断片の長さによる種判別
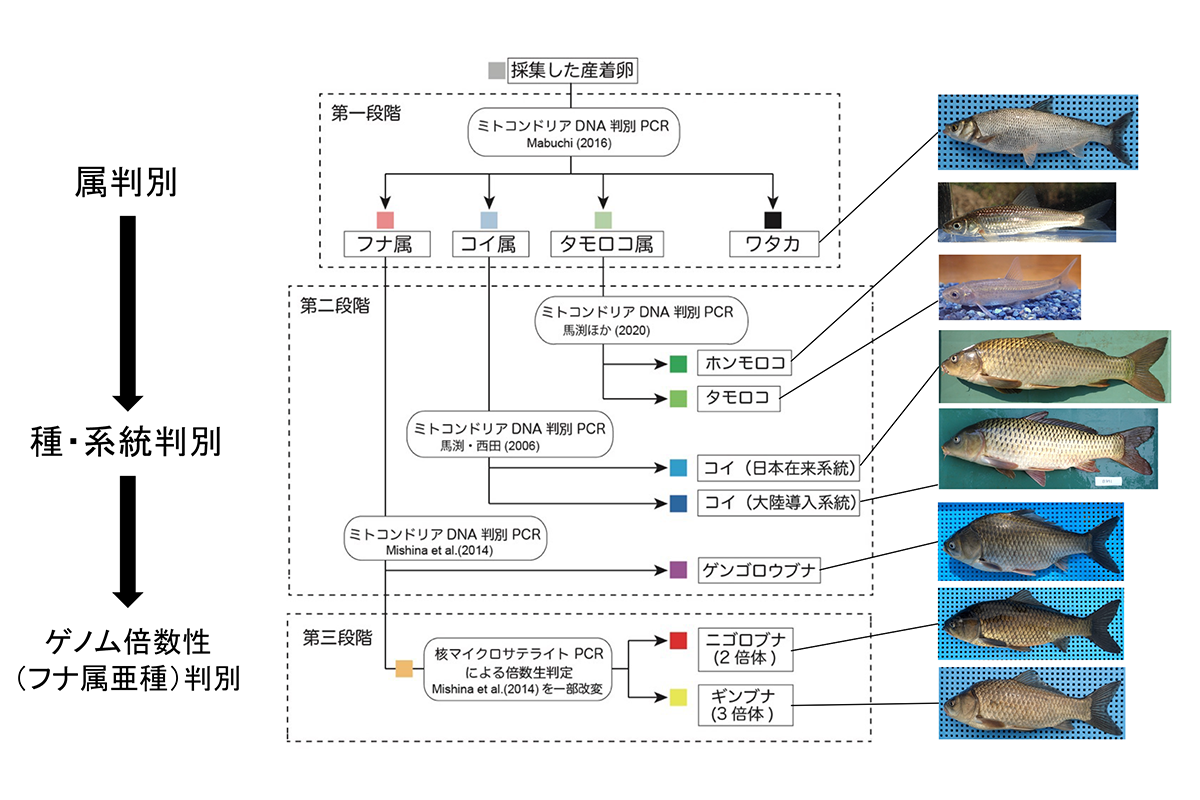
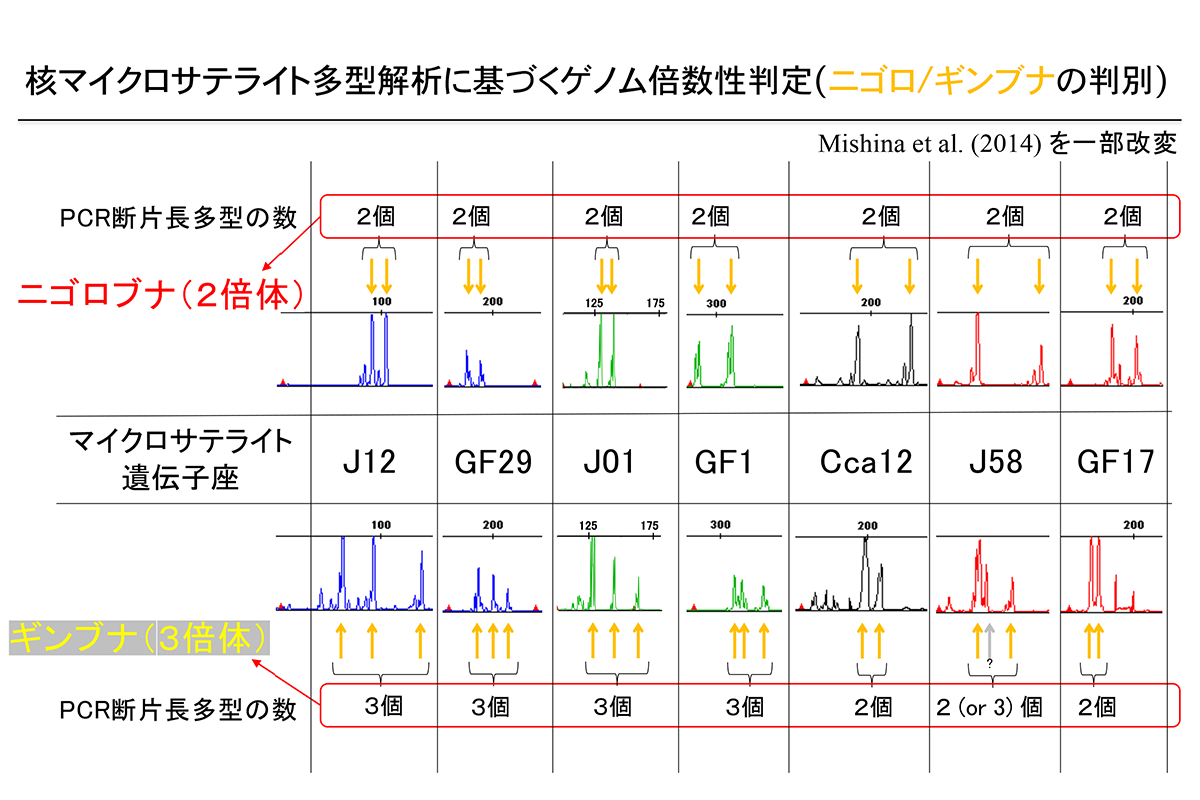
琵琶湖とその周辺において、水面近くの植物体(葉、茎、根)や浮遊物等に高い密度で卵を産み付ける魚には、コイ、フナ、ホンモロコの仲間のほかワタカが存在します。採集した卵がこれらの内のどの魚種のものかを簡便に判定するため、各グループを識別できる塩基サイトにアリル特異的プライマーを設計しました。このプライマーでPCR増幅されるDNA断片の大きさによって属や種・系統を段階的に判別できるようにしています(図4a,b)。なお、ニゴロブナ(2倍体)とギンブナ(3倍体)はミトコンドリアDNAでは区別できないため、マイクロサテライト多型を用いた核ゲノムの倍数性判定(図4c)により区別しています。実験手法の詳細についてはこちらのPDF をご覧ください。

(b) 部分塩基配列の決定による種判別
水底の石や石垣の隙間などに産み付けられている卵は、コイ、フナ、ホンモロコやワタカ以外の魚種の卵である可能性があります。そこで、汎用性の高いプライマーでミトコンドリアDNAの部分塩基配列を増幅し、塩基配列を決定してデータベース上でBLAST検索することにより魚種を判別します。また、上記の(a)の方法でPCRがうまくいかなかったものの一部についても、この方法で種判別する場合があります。得られた部分塩基配列や解析に用いたプライマーの情報は、個々の卵の項に掲載しています。プライマーの塩基配列とPCR条件等については「プライマー情報 」をご覧ください。